Keywords
Basal ganglia; Hyponatremia; Myelinolysis; Extrapontine myelinolysis; Parkinsonism; Movement disorder
Introducción
El parkinsonismo o síndrome parkinsoniano ocurre por afectación nigro-estriatal y clínicamente se define por la presencia de bradicinesia más temblor y/o rigidez [1,2]. Existen múltiples causas que pueden provocar éste síndrome, por ejemplo: anoxia, intoxicaciones, isquemia, causas metabólicas, entre otras. Sin embargo, la enfermedad idiopática de Parkinson es la causa más común. La importancia de diferenciar la enfermedad idiopática de Parkinson del parkinsonismo secundario radica en que este último no responde adecuadamente a la terapia sustitutiva dopaminérgica o lo hace de forma leve y transitoria, además el pronóstico del paciente difiere según la enfermedad que lo provoca [1,3].
El síndrome de desmielinización osmótica (SDO), es una causa rara de parkinsonismo secundario que se caracteriza por la desmielinización de la sustancia blanca provocada por cambios bruscos de osmolaridad en el sistema nervioso central [4-6]. También se denomina mielinolisis pontina y extrapontina dependiendo si la desmielinización se limita o no a la protuberancia; puede desarrollarse en pacientes con hiponatremia donde la corrección de sodio suele ser mayor a 12 mEq/L en 24 hrs [5,7].
Las manifestaciones clínicas que se han descrito son variables, puede presentarse como un cuadro confusional agudo o subagudo. La mielinolisis centro-pontina (MCP) cursa frecuentemente con síntomas cortico-espinales, corticobulbares y/o enclaustramiento. La afectación extrapontina (MEP) es menos frecuente y se ha señalado su afectación en los ganglios de la base, mesencéfalo, tálamo, cerebelo y substancia blanca paraventricular. Al verse afectado el tracto extrapiramidal se han descrito la presencia de movimientos anormales como ser parkinsonismo, corea, distonias y/o mioclonias [8,9]. Ante la sospecha clínica, el diagnóstico se confirma con los hallazgos de cambios desmielinizantes en la base del puente y en ocasiones en áreas extrapontinas visualizados en estudios de imagen, siendo el de elección la imagen por resonancia magnética (IRM) [7].
Actualmente no hay un tratamiento específico, solo sintomático; en caso de afectación extrapiramidal se han reportado algunos casos con respuesta favorable a fármacos dopaminérgicos [10,11]. El enfoque terapéutico debe ser la prevención-evitando realizar reposiciones rápidas de sodio plasmático; además brindar terapia coadyuvante de rehabilitación para las secuelas neurológicas [5,6].
Se describe el caso de un paciente que presentó parkinsonismo secundario a mielinolisis pontina y extrapontina, por reposición rápida de sodio.
Caso Clínico
Paciente masculino de 47 años, con antecedente de hiperplasia prostática benigna con uso de catéter urinario intermitente; quien acudió a la sala de emergencia por un cuadro febril de 3 días de evolución, oliguria y confusión. Ingreso con cuadro confusional (escala de Glasgow 13/15), febril (temperatura 39?C), presión arterial 80/60 mmHg, taquicardico, taquipneico y globo vesical palpable. Cumpliendo criterios clínicos de choque séptico ya que recibió reposición de volumen con soluciones isotónicas sin recuperar cifras tensionales, se admitió a la unidad de cuidados intensivos y se inició infusión de dopamina y posterior a toma de muestra para cultivos de orina y sangre recibió cobertura antibiótica empírica para infección del tracto urinario complicada en pacientes con uso de catéter urinario. Al tener resultados de laboratorio resalta hiponatremia severa (101 mEq/L), hipopotasemia, creatinina elevada (2.3 mg/dl), uroanálisis con hematuria, piuria, nitritos positivos y estereasa leucocitaria positiva, gasometría con acidosis mixta e hipoxemia.
El paciente evolucionó satisfactoriamente del cuadro infeccioso, pero sin mejoría cuadro confusional por lo que se realiza punción lumbar la cual no reveló datos de neuroinfección, con cultivos bacterianos y PCR para Herpes virus negativos. Posteriormente es presentado al servicio de neurología por presentar temblor en reposo bilateral y bradicinesia al examen neurológico se encuentran movimientos sacádicos verticales lentos, bradicinesia global, rigidez en rueda dentada de las cuatro extremidades además temblor en reposo bilateral de ambas manos; ante la presencia de un cuadro claramente parkinsoniano se utiliza y se aplica la escala unificada para la enfermedad de Parkinson (UPDRS III por sus siglas en ingles) de 38 puntos con escala Hoehn y Yahr grado II; ante un cuadro parkinsoniano agudo con disnatremia se sospechó mielinolisis pontina central y extrapontina, por lo que se solicita IRM y se observó alteraciones de la señal a nivel pontino y en ganglios de la base (Figura 1-3). Se dio manejo con levodopa/ carbidopa a dosis escalonada hasta llegar 1000 miligramos/día, con una respuesta parcial del 14% en relación al UPDRS basal.
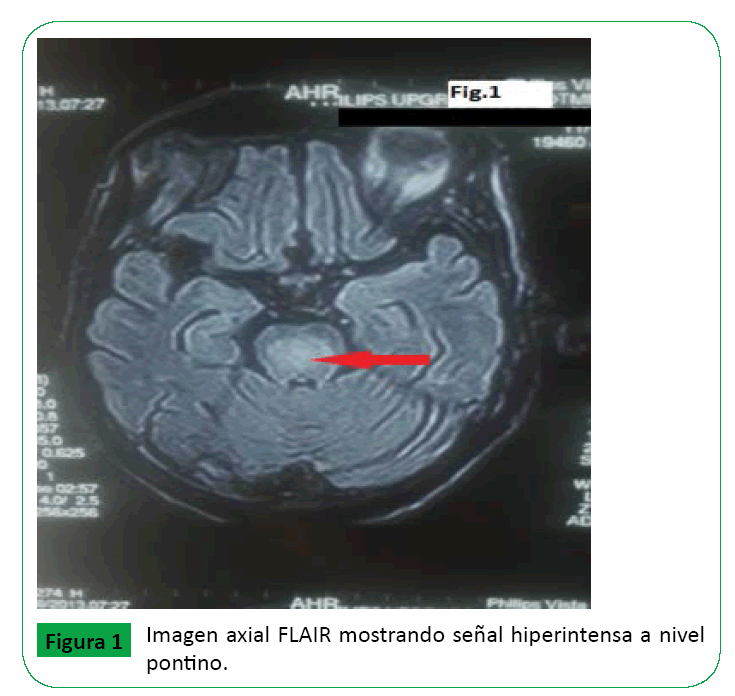
Figure 1: Imagen axial FLAIR mostrando señal hiperintensa a nivel pontino.
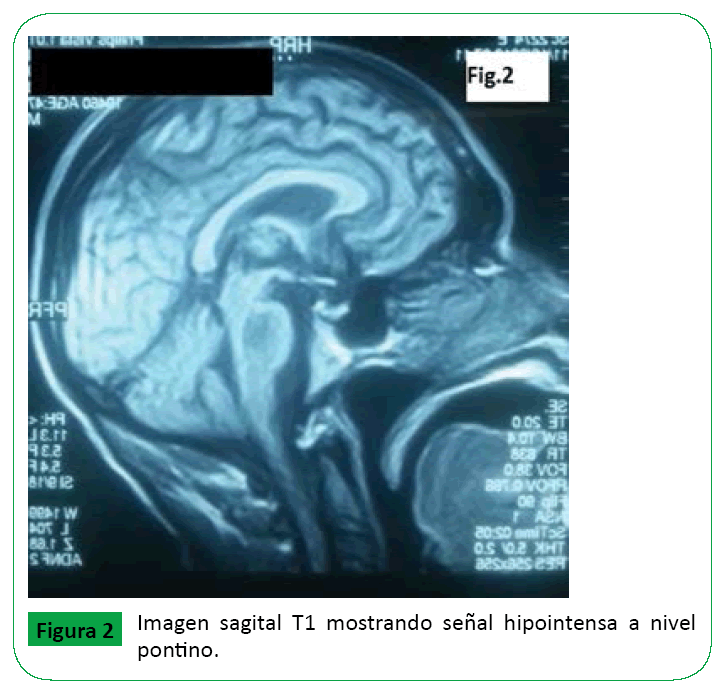
Figure 2: Imagen sagital T1 mostrando señal hipointensa a nivel pontino.
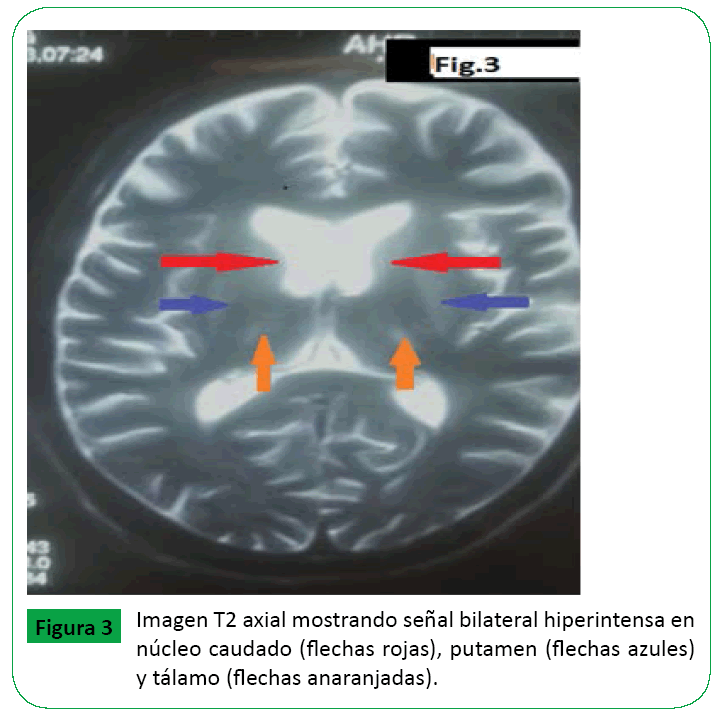
Figure 3: Imagen T2 axial mostrando señal bilateral hiperintensa en núcleo caudado (flechas rojas), putamen (flechas azules) y tálamo (flechas anaranjadas).
Discusión
El parkinsonismo o síndrome parkinsoniano se refiere a un cuadro clínico caracterizado bradicinesia, temblor en reposo y/o rigidez [12]. Existen varias circunstancias clínicas que pueden desencadenar estas manifestaciones al producir una alteración en la vía nigro-estriatal, ya sea por una enfermedad degenerativa u otra afectación en la cual exista una lesión en el sistema extrapiramidal; también puede presentarse por el uso de determinados fármacos que bloquean los receptores dopaminérgicos principalmente los D2 [1,2].
Ante un paciente con cuadro clínico de parkinsonismo, lo primero es distinguir la enfermedad idiopática de Parkinson, causa más común de síndrome parkinsoniano, de un parkinsonismo secundario. Para ello es necesario un abordaje exhaustivo debido que el pronóstico y respuesta terapéutica varía en ambas [1,3,12]. Se sospecha parkinsonismo secundario cuando las manifestaciones clínicas aparecen de forma aguda, la presentación es muy simétrica o con asimetría muy marcada, se acompaña de "red flags", signos piramidales, cerebelosos, debilidad, mioclonias, etc., así como el no tener respuesta clínica con dosis elevadas de levodopa (1000 mg/día) por un mes. Entre las causas secundarias infrecuentes de parkinsonismo está el SDO. Han sido descritos pocos casos de ésta condición. En estos pacientes hay lesiones extrapontinas evidenciadas en estudios de imagen, siendo el de elección la IRM [10,13,14]. Entre los diagnósticos diferenciales se puede incluir isquemia, anoxia, intoxicaciones, enfermedades infecciosas, entre otras [15]. Éstas últimas presentan un curso y sintomatología variada en relación a la desmielinizacion pontina y extrapontina, por lo que se pudo excluir estas condiciones.
El SDO se caracteriza por la presencia de lesiones simétricas, circunscritas, agudas o subagudas causadas por desmielinizacion no inflamatoria. Las áreas afectadas se clasifican en centropontina, que representa la mitad de los casos y extrapontina, que representa el 20%. En el 30% restante se encuentran lesiones en ambas áreas [8], como se describe en el caso con señales simétricas en puente, núcleo caudado, putamen, tálamo y mesencéfalo. Esta condición representa el 0.4%-0.56% de las admisiones en las salas de neurología [16].
Adams en 1959 describió en un paciente alcohólico lo que actualmente se conoce por SDO. Se sabe que ocurre por cambios en la osmolaridad a consecuencia de correcciones rápidas de desbalances electrolíticos y sucede frecuentemente en pacientes con hiponatremia crónica, pero puede presentarse en la corrección de la hipernatremia o con menor frecuencia en otras entidades que afecten bruscamente la osmolaridad [16]. En la revisión de reporte de caso publicado por Singh et al. en 2014, el 74.3% de los pacientes cursaron con hiponatremia de los cuales el 22.8% cursaron con hiponatremia severa, definiendo severa como un valor menor de 120 mEq/L, como es el caso que al ingreso presentó un valor inicial de 101 mEq/L [9].
La fisiopatología aún no es clara, una de las hipótesis con mayor aceptación plantea que la neuroglia tiene una reducida respuesta ante cambios bruscos de concentración de iones, causan estrés en las células y disminuye su capacidad de funcionamiento [8]. En alcohólicos, el alcohol altera la homeostasia de agua y sodio por interferencia en el funcionamiento de la hormona antidiurética [15].
Las manifestaciones clínicas neurológicas son variables y muestran un curso bifásico, el 44-50% de los pacientes presentan parkinsonismo como primer signo y el 16% lo presentan tardíamente como es el caso del paciente que inició con un estado confusional que en un principio se atribuyó a la hiponatremia severa.
La MEP es una causa rara de parkinsonismo secundario, como resultado de la deficiencia de dopamina debido a la reducción del transportador presináptico de dopamina y receptores a nivel estriatal [8,9,16]. Se han reportado casos de afectación extrapiramidal que responden favorablemente a fármacos dopaminérgicos, a pesar de que solo existe tratamiento sintomático y no uno específico [4,11].
Por lo anterior expuesto, el parkinsonismo secundario, como consecuencia de una injuria osmótica por desbalance electrolítico, es una complicación poco frecuente la cual tiene una respuesta terapéutica variable. Con una presentación aguda o subaguda y con manifestaciones clínicas bilaterales de un síndrome motor Parkinsoniano se debe hacer un abordaje exhaustivo en busca de una causa secundaria ya que la respuesta a la terapia sustitutiva dopaminérgica difiere en comparación a la enfermedad de parkinson idiopática. Conflicto de Interés
Conflicto de Interés
Los autores declaran no tener conflictos de interés en la publicación del presente artículo.
11384
References
- Hanagasi HA, Aygun D, Tufan F, Babacan G, Gurvit H, et al. (2009) P2.071 ExtrapontineMyelinolysis after Correction of Hyponatremia Presenting as Acute Parkinsonism. Parkinsonism Relat D 15: S107-S108.
- Seah ABH, Chan LL, Wong MC, Tan EK(2002) Evolving Spectrum of Movement Disorders in Extrapontine and Central Pontine Myelinolysis. Parkinsonism RelatD 9:117-119.
- Ho B, Apetauerova D, Thomas C, Arle J, Russell JA (2006) Reversible extrapontine and central pontinemyelinolysis presenting with extrapyramidal features. MovDisord 21:585-586.
- Juergenson I, Zappini F, Fiaschi A, Tonin P, Bonetti B (2012) Teaching neuroimages: neuroradiologic findings in pontine and extrapontinemyelinolysis: clue for the pathogenesis?Neurology 78:e1-e2.
- Huq S, Wong M, Chan H, Crimmins D (2007) Osmotic demyelination syndromes: central and extrapontinemyelinolysis. J ClinNeurosci 14:684-688.
- Garzon T, Mellibovsky L, Roquer J, Perich X, Diez-Perez A (2002) Ataxic form of central pontinemyelinolysis. Neurology 1:517-518.
- Madey JJ, Hannah JA, Lazaridis C (2013) Central pontinemyelinolysis following acute hypoglycemia. ClinNeurolNeurosurg115:2299-2300.
- Dujmovic I (2016) Central Pontine Myelinolysis in Alcoholism. In:Neuropathology of Drug Addictions and Substance Misuse: Elsevier. pp: 600-609.
- Singh TD, Fugate JE, Rabinstein AA (2014) Central pontine and extrapontinemyelinolysis: a systematic review. Eur J Neurol21:1443-1450.
- Sajith J, Ditchfield A, Katifi HA (2006)Extrapontinemyelinolysis presenting as acute parkinsonism. BMC Neurol 6: 33.
- Toft M, Dietrichs E (2011) Levodopa-responsive parkinsonism in probable extrapontinemyelinolysis of the mesencephalon. MovDisord 26:2180-2181.
- Jiménez-Jiménez FJ, Alonso-Navarro H, Luquin-Piudo MR, Burguera-Hernández JA (2007)Trastornos del movimiento (I): conceptosgenerales. Clasificación de los síndromesparkinsonianos yenfermedadde parkinson. Medicine 9:4719-4729.
- Sullivan AA, Chervin RD, Albin RL (2000) Parkinsonism after correction of hyponatremia with radiological central pontinemyelinolysis and changes in the basal ganglia. J ClinNeurosci 7: 256-259.
- Souza A (2013) Movement Disorders and the Osmotic Demyelination Syndrome. Parkinsonism RelatDisord19:709-716.
- Zahr NM, Kaufman KL, Harper CG (2011) Clinical and pathological features of alcohol-related brain damage. Nature reviews. Neurology 7:284-294.
- Kim J, Lee K, Han S, Chung Y (2003) Decreased Striatal Dopamine Transporter Binding in a Patient with ExtrapontineMyelinolysis. MovDisord18: 342-344.








